Molécule d'acide
Un acide consiste en un ou plusieurs atomes d'hydrogène liés de manière covalente avec un autre non-métal ou groupe de non-métaux (on parle alors d'ion polyatomique). Comme l'hydrogène est un des moins électronégatifs de tous les non-métaux, son électron est très attiré par le non-métal auquel il est lié. Il en résulte une molécule avec un moment polaire, positif sur l'hydrogène et négatif sur le non-métal voisin.
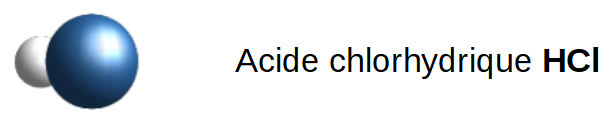
En général, la formule d'un acide indique d'abord le ou les H pour hydrogène, suivi de sa base conjuguée (ce qui reste une fois l'hydrogène enlevé):
Acide chlorhydrique: HCl → H+ + Cl-
Acide sulfurique: H2SO4 → 2 H+ + SO4-
Exceptions notables: acide acétique (vinaigre) CH3COOH, acide citrique C6H8O7.
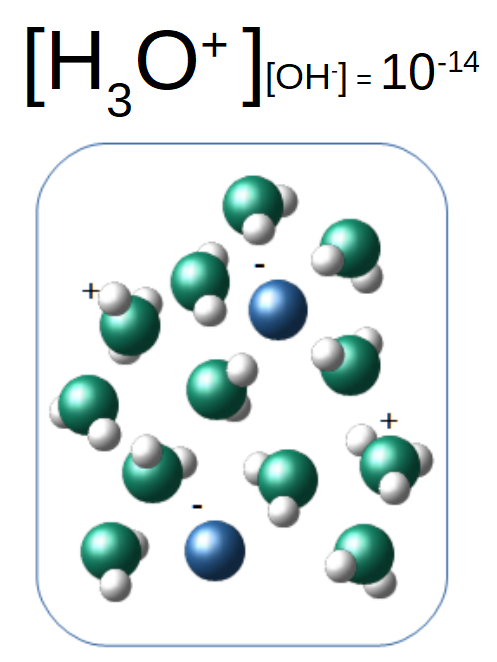
Placé parmi des molécules d'eau, un acide peut perdre son hydrogène au profit de l'eau. Cet hydrogène est alors pris par une molécule d'eau, qui devient de l'hydronium H3O+. Comme un ion négatif vient avec l'acide, la solution reste électriquement neutre.
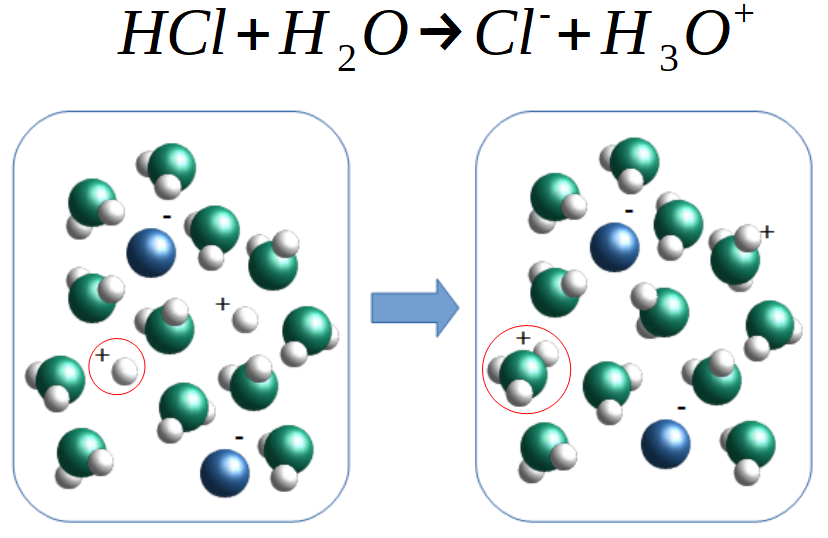
Le nombre d'hydroniums augmentant, et le produit ionique de l'eau restant constant, la concentration en hydronium augmente et celle en hydroxyde baisse. On dit alors de la solution qu'elle est acide.