Hydroxyde d'un métal
Une base est le plus souvent un composé ionique: un ou plusieurs atomes d'un métal couplé à un ion polyatomique: l'ion hydroxyde OH-.
En général, une base est une substance qui retire un atome d'hydrogène à l'eau. Dans le cadre de ce cours, nous nous limiterons aux bases composées d'un métal et d'un hydroxyde.

Lorsque dissous dans l'eau, un hydroxyde d'un métal alcalin ou alcalino-terreux (deux premier groupes du tableau périodique) se décompose en un cation (le métal, ion positif) et un anion (l'hydroxyde).
Ce dernier peut prendre un atome d'hydrogène à une molécule d'eau voisine, qui elle-même devient un ion hydroxyde. Le résultat est qu'une base augmente la quantité d'ions hydroxyde dans une solution.
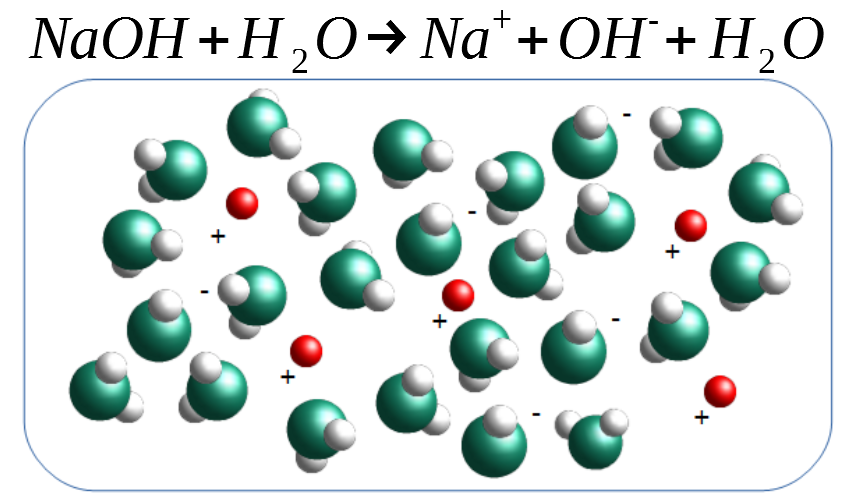
Le produit ionique de l'eau restant toujours constant, une augmentation des ions hydroxydes mène à une augmentation de leur concentration.
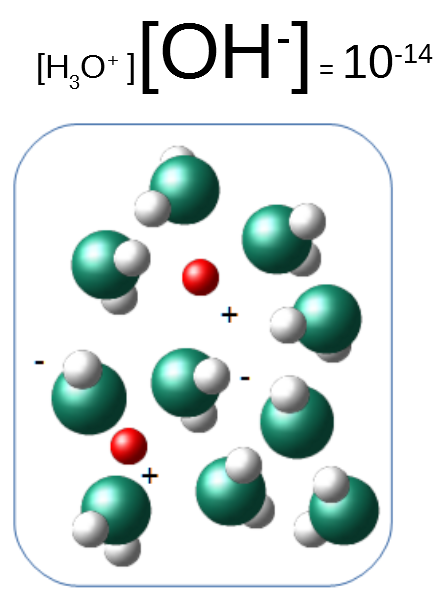
On en conclut qu'une base prend un hydrogène à l'eau, et augmente sa concentration en ions hydroxydes. A l'inverse, un acide donne un hydrogène à l'eau et augmente sa concentration en ions hydroniums.